技術職員が実現!マウス実験の革新技術
「もともと手先は器用でして」と、はにかみながら話すのは、国立遺伝学研究所の技術職員で令和6年度文部科学大臣表彰 研究支援賞に輝いた木曾 誠さんだ。繊細さが求められる遺伝子や細胞の操作、マウスの扱いに熟練した木曾さんだからこそ、確立できた新技術。ベテラン研究者が絶大な信頼を寄せ、若手研究者が気兼ねなく頼る、屋台骨としての姿。先端研究を強力に支える「陰の立役者」に迫る。

答える人:木曾 誠 班長 (国立遺伝学研究所)
きそ・まこと。国立遺伝学研究所 技術課 基盤支援技術班 班長。民間企業の医薬情報担当者、食品開発職を経て、国立医薬品食品衛生研究所でマウス作製技術を習得。2001年より国立遺伝学研究所の技術職員。ゲノム変異マウスの開発支援業務に従事し「1世代遺伝学を可能にしたキメラマウス解析技術確立への貢献」で令和6年度文部科学大臣表彰 研究支援賞を受賞※1。
200匹必要だったマウスが10匹に
実験生物の代表格、マウス。基礎研究から安全性評価に至るまで、理・農・薬・医・歯学の幅広い分野に用いられ、我々が受けている恩恵は計り知れない。
マウスを用いる代表的な研究手法の一つに、ノックアウトマウスの作製がある。特定の遺伝子を破壊(ノックアウト:KO)し、欠損させることで、どんな異常が現れるのかを調べる。その遺伝子が何に寄与しているのか、表現型から遺伝子の機能を探る、逆遺伝学のアプローチだ。
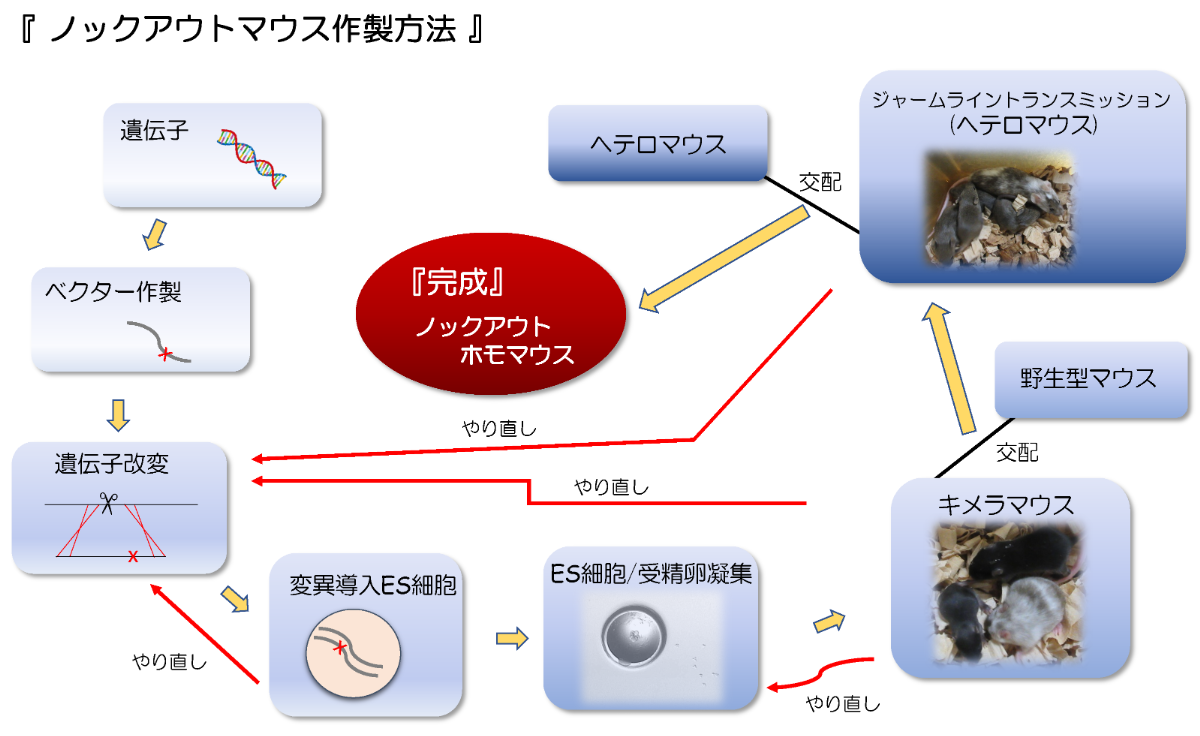
標的となる遺伝子が決まり、マウスにその欠損を導入するまでを図1に示す。まずターゲッティングベクターという遺伝子導入のツールを設計し、目的の遺伝子をピンポイントで壊すための【目印】を仕込んでおく。そのターゲッティングベクターをマウスのES細胞に特殊な試薬で導入すると、目的の遺伝子が改変されたターゲッティングベクターと組み換わったES細胞が得られる。
ES細胞を使うのは、あらゆる細胞に分化できる多能性幹細胞だからだ。受精後2.5日目の8細胞期胚に組み換えたES細胞を取り込ませて、代理母マウスの子宮に移植する。こうして生まれた仔にはES細胞と8細胞期胚、両方に由来する細胞が混在している。これがキメラマウスだ。

キメラマウスでES細胞が生殖細胞に入れば、交配の後、次世代にES細胞由来のKOマウスが得られる──というわけだが、実際はそう簡単ではない。
「1回の出産で狙い通りのマウスが生まれてくるとは限りません。ES細胞由来の遺伝子配列が次世代に引き継がれなければ、やり直しです。ES細胞が生殖細胞に入っているかを確認するため、キメラのオスと野生型のメスを交配する必要もあります。そのうえ2個以上の遺伝子改変を同時に持つマウスを作製する場合や、発生のある時期、特定の組織で発現する遺伝子を狙う条件付きノックアウトマウスの解析になると、数百匹のマウスが必要になるのです」
そう話すのは、国立遺伝学研究所(遺伝研)で基盤支援技術班班長を務める木曾 誠さんだ。
条件付きKOマウスは、通常のノックアウトマウスでは発生の初期に胎生致死で解析が困難な遺伝子を特定の時期や組織で機能解析する目的で近年盛んに用いられている。だが、作製には1~2年以上かかり、そこに至るまでのマウスも200~500匹に及ぶ。
そこで木曾さんらは、「キメラ胚」を利用することで、遺伝子改変マウス同士を交配しなくとも、条件付き遺伝子KOを解析できる新たな手法を検討。所要時間は4カ月、必要なマウスは10~20匹と大幅な効率化を実現。これが「1世代遺伝学を可能にしたキメラマウス解析技術」だ。
大胆な発想と、繊細な技術
「この手法が使えるのは、主に胎児での影響を見たい場合」と木曾さんは前置きするが、それでも時間勝負の研究の世界でインパクトは絶大だ。犠牲となるマウスも大量に減る。飼育にかかる費用・スペースも抑えられる。では、なぜ従来法は多くの時間とマウスを要するのか。
先ほど条件付きKOマウス作製の流れを示したが1つの系統を用意するだけでも、最低5カ月はかかる。だがそれはゴールではなく、スタートライン。遺伝子をKOし、それを確かめるには、少なくとも3つのツールが必要だ。KOする遺伝子を挟む【目印: lox】、その目印でDNA配列を切る【ハサミ: Cre】、KOされたことを示す【マーカー: GFP】。それぞれの遺伝子を持ったマウスが揃って、ようやく本題に入る。
ここから3段階の掛け合わせを経て、最終的に3種類すべての遺伝子が全て入ったマウスが得られるまでが1~2年。メンデルの法則を思い浮かべるとイメージしやすいかもしれないが、組み合わせのバリエーションが増えるほど、目的外のマウスもどうしても多くなってしまう。
「導入したい遺伝子配列を次世代に引き継いでいくために、ES細胞由来の精巣を持つオスを起点に掛け合わせていきます。でも当然、遺伝子配列は同じでも、メスが生まれることもあります。また、最終的に目的とするKOマウスも1匹では足りません。総じてマウスの量も、時間も膨大になってしまうのです」
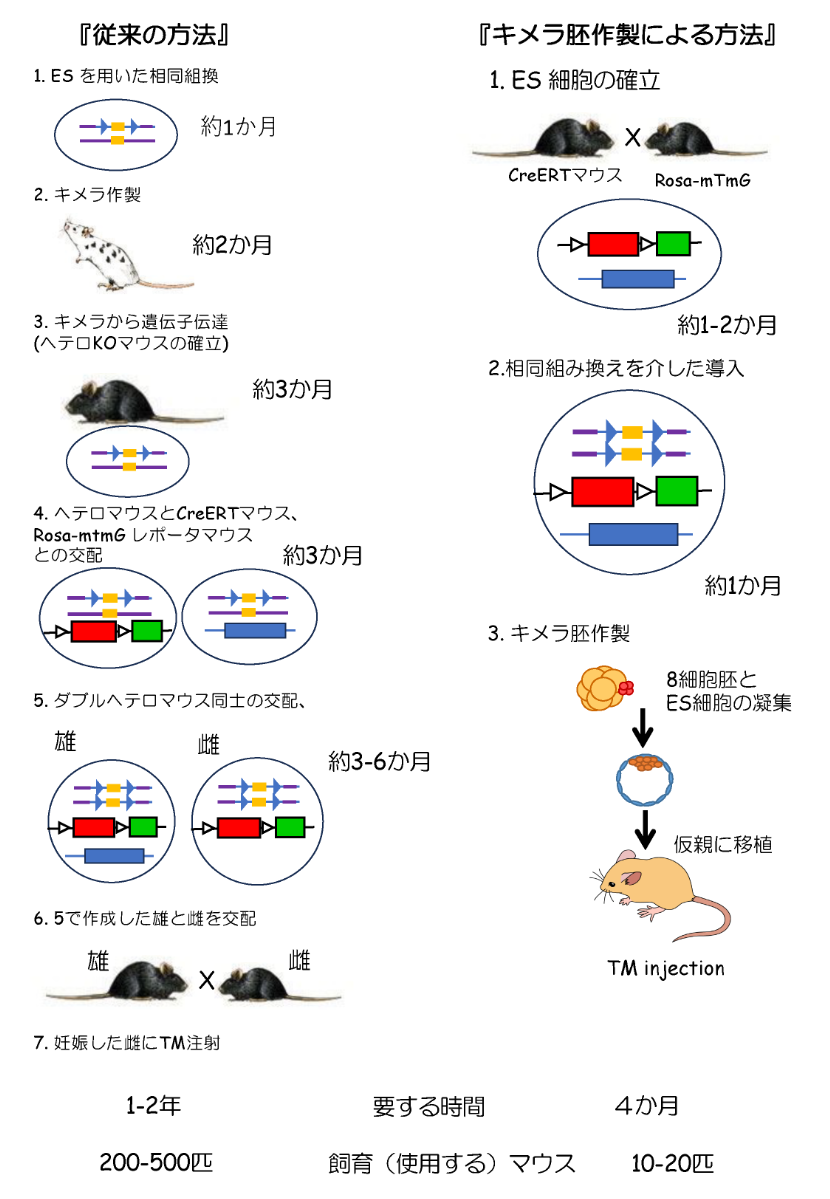
そこで最低でも3段階は必要だった掛け合わせを、1段階で済むようにしたのが「キメラ胚」の利用だ※2。戦略としては、まず【マーカー】と【ハサミ】を持ったES細胞を先に樹立しておく。そのために、先ほど同様2種の【マーカー】を導入したマウスと、時期・組織を選んで機能する【ハサミ】の遺伝子を持ったマウスを交配させ、その受精卵からES細胞を得る。
次に、ターゲッティングベクターを作り(その点は同じ)、このES細胞に導入する。ここで標的の遺伝子がベクターのものと組み換われば【マーカー】【ハサミ】【目印】の3点が揃う。このES細胞と、8細胞胚を凝集させたものがキメラ胚である。キメラ胚を培養した後、胚盤胞まで発生したものを代理母に移植し発生させたものがキメラマウスだ。あとは確認したい発生の段階で胎児を取り出し、解析する。
もちろん「キメラ」なので胎児の全細胞で遺伝子がKOされているわけではない。だが、同一個体内で、ホスト胚由来の正常細胞と、ES細胞由来のKO影響をまったく同じ条件で比較できる──というロジックなのだが、果たして代替法として成立するのか。その実証を託されたのが、木曾さんだった。

先端バイオテクノロジーに光る職人技
従来法と新手法、いずれにしても欠かせないのがES細胞の樹立、そして8細胞期胚との凝集だ。図1でも示したように遺伝子がKOされるように設計したターゲッティングベクターと組み換えが起こったES細胞を8細胞期胚に取り込ませることが、キメラ胚やキメラマウスの作製には不可欠だ。
どうやって取り込ませるのかと言えば、なんと手作業。「受精卵が細胞分裂を繰り返し、8個の細胞に分割した8細胞期胚に、ES細胞を凝集させると、胚が自然にES細胞を取り込みます。ただ、マウスの8細胞期胚は約100μm(0.01㎝)です。そこに、さらに小さな10μmのES細胞を手作業で付けるのは、なかなかの職人技かもしれませんね」と木曾さん。

実はES細胞の未分化状態を保つのも、一苦労だという。「毎日、培養液を交換するなど、ルールを徹底してもシャーレの中でES細胞が分化してしまうことに悩まされていました。そうなれば、キメラ胚、キメラマウスも作れません。かなり時間がかかりましたが、やっと状態の良いES細胞に出合えたことで、ES細胞寄与率の高いキメラマウスが作製できるようになりました」。
何か一つでも、ほんの僅かに条件が変わるだけで、結果が左右される実験科学。成長の早いマウスを発育のタイミングを狙って解析するのも容易ではない。ES細胞の樹立、遺伝子導入、キメラ胚の作製と一連の過程において、常に高い精度を保ち、安定して実験を行えるようにする「確かな技術力」があってこそ、革新的なロジックが証明できたと言えるだろう。
民間企業から研究機関、そして遺伝研へ
研究者から厚い信頼を寄せられる木曾さんだが、ずっと研究の世界にいたわけではなかった。
「大学では細胞工学を専攻し、修士課程を修了して製薬企業に就職しました。希望は研究開発職でしたが、入社後の研修を経て配属が決まるシステムで、私は医薬品情報担当者(MR)として働くことになりました。でも、やはり研究分野に携わっていたかったのです。食品会社の開発部門に転職した後も、大学で学んだことを生かしたいという気持ちが消えませんでした。そんな時、偶然、見つけたのが、新聞に小さく掲載されていた国立医薬品食品衛生研究所のテクニシャンの募集でした」
その採用面接で、木曾さんは相賀 裕美子先生(現・遺伝研 名誉教授)と出会う。正社員を辞めて、派遣会社に登録し、出向する形での採用だったが、木曾さんに迷いはなかった。食品会社で業務の引継ぎなどを済ませた2カ月後、その日を迎えた。

「相賀先生に挨拶に行った初日、こう言われたんです。『私、教授として遺伝研に移ることになったの。あなた、どうする?』って。でも迷いはありませんでした。『行きます!』と即答でした」。この時、相賀先生に言い渡された“宿題”は、半年間でES細胞からKOマウス作製までをマスターすること。木曾さんは懸命に“修行”を積み、ついに遺伝研に着任。
ここでまた、木曾さんは恩師との再会を果たす。大学・大学院時代の指導教官だった黒田行昭先生が、名誉教授として遺伝研に在籍していたのだ。木曾さんは黒田先生のもとで、細胞培養の基礎を身に着け、動物実験の代替法として、細胞の有用性を学んでいた。
「HeLa(ヒーラ)細胞という一人の子宮頸がん患者さんから得られた細胞株が、世界中の医学研究に使われていることに衝撃を受けました。細胞で代替できない場合もありますが、新しい技術を取り入れることで、動物の犠牲を減らせる方向に考えられるときはホッとします」

研究を支えるプロフェッショナル人材
日々、誰よりも近くで、誰よりも注意深くマウスに接している木曾さんだからこそ、成しえた発見もあった。なんと脱毛の原因遺伝子を突き止めたのだ※3。
「全く別の目的で作製を依頼されたマウスなんですが、なぜだか毛が抜けてしまって。異変を報告したところ、本来の解析対象ではないので、興味があれば調べてもらって構わないですよ、と。相賀先生にも『あなたが見つけたんだから、自分で調べてみたら』と背中を押してもらえたので、技術職員の仕事と並行で、これに関しては私が中心となって研究を進め、論文にまとめることができました」
自ら研究する経験も経て、木曾さんは技術職員の役割をこう語る。
「遺伝研での我々のポジションは任期制ではないので、研究室の主催者(PI)の次に長く研究室に在籍することになります。一方で、研究者は学生、ポスドク、助教と移籍しながらキャリアを積んでいきます。ただそれを見送るだけでなく、彼らが持つ知見・技術を研究室に蓄積しながら“引き出し”を増やし、新たなメンバーへと継承してく。それも私の役目だと思っています。そのためには、時にはぶつかり、時には飲み明かし、と日々のコミュニケーションが大切です。一つでも多くのことを吸収してもらいたいですし、困った時には頼ってもらえる関係性を築きたいですね。近年希薄になりがちなコミュニケーションですが、あえてそこは踏み込んでいきます」

巣立ったOBが新たに自分の研究室を立ち上げ、数年ぶりに、時には海外から実験作業のノウハウを知りたいと連絡をもらうこともあるという。自ら研究の喜びや苦しみも感じたからこそ、日々の実験支援も、長期的な研究支援も「頼んで良かったと思ってもらえる仕事をしていきたい」。木曾さんは力強く語った。
※1 技術課・木曾誠班長が令和6年度文部科学大臣表彰 研究支援賞を受賞
※2 Ryuki Shimada et al. (2019) ES-mediated chimera analysis revealed requirement of DDX6 for NANOS2 localization and function in mouse germ cells. Scientific Reports. 9(515)
DOI:10.1038/s41598-018-36502-0
※3 Makoto Kiso et al. (2009) The disruption of Sox21-mediated hair shaft cuticle differentiation causes cyclic alopecia in mice. PNAS.106 (23) 9292-9297.
DOI: 10.1073_pnas.0808324106
(聞き手:サイエンスライター 堀川晃菜 写真:飯島雄二 公開日:2025/3/25)




